Siempre hemos sentido curiosidad: ¿cómo funcionan exactamente las neuronas del cerebro? Antes de la tecnología de imagen avanzada, era como mirar el mundo a través de un cristal esmerilado: borroso, superficial y dañino para las muestras. Entonces surgió una «combinación dorada»: microscopía de dos fotones + imagen de calcio + sistema de fijación de cabeza, que permitió a los científicos ver por primera vez un cerebro vivo, despierto y pensante.
¿Por qué los microscopios convencionales no pueden ver un cerebro vivo?
Limitaciones de la microscopía de fluorescencia tradicional
🔻 La luz ilumina toda la capa → fuerte ruido de fondo
🔻 Cuanto más grueso el tejido, menos se ve → profundidad de imagen limitada
🔻 La iluminación prolongada daña las células → alta fototoxicidad
Los requisitos fundamentales de la neurociencia son precisamente: obtener imágenes de tejido vivo, en profundidad, durante periodos prolongados, capturando actividad real. La microscopía tradicional simplemente no puede hacerlo, hasta la llegada de la microscopía de dos fotones.
1. Microscopía de dos fotones — La revolución óptica en la imagen cerebral
Principio fundamental — Dos fotones débiles excitan fluorescencia simultáneamente en lugar de un fotón fuerte
- Fluorescencia convencional: 1 fotón de alta energía → capa aleatoria → toda la capa fluoresce
- Dos fotones: 2 fotones de baja energía → deben impactar el mismo punto simultáneamente → solo entonces se excita la fluorescencia
La probabilidad de que dos fotones coincidan en tiempo y espacio es extremadamente baja (requiere superposición en 10-16–10-18 segundos), y solo ocurre en la diminuta región focal del láser. Por eso los microscopios de dos fotones exigen fuentes de luz excepcionales. El láser principal utilizado hoy es el láser pulsado de femtosegundo de titanio-zafiro, que emite pulsos ultradensos a escala de femtosegundo, aumentando drásticamente la probabilidad de excitación simultánea de dos fotones en el punto focal. La aparición del láser de femtosegundo fue lo que convirtió la imagen de dos fotones en una realidad práctica.
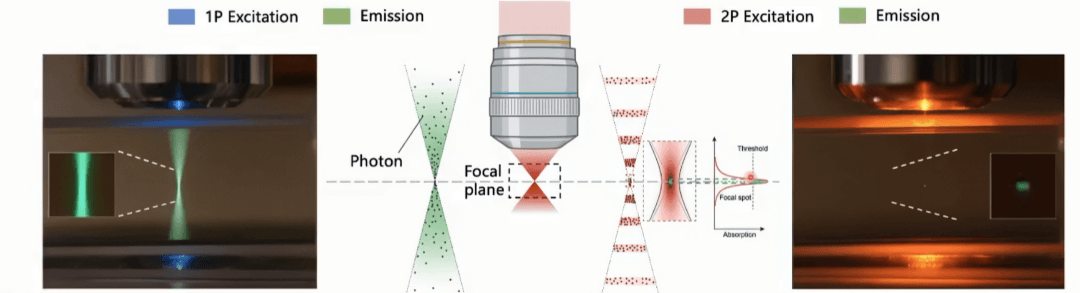
Fuente de imagen: «1P vs 2P fluorescence imaging» por Steve Ruzin y Holly Aaron
Uso exclusivo con fines académicos y educativos. Contáctenos para su eliminación si es necesario.
Características clave de la imagen de dos fotones
- Seccionamiento óptico intrínseco: No se necesita pinhole confocal — capacidad integrada de escaneo capa por capa.
- Fondo casi nulo: Las regiones fuera del foco permanecen completamente oscuras, produciendo imágenes excepcionalmente limpias.
- Imagen 3D real: Variando la profundidad focal, se pueden escanear capas secuenciales y reconstruir estructuras cerebrales en 3D.
¿Por qué la microscopía de dos fotones usa láseres de infrarrojo cercano? (650–1100 nm)
La luz infrarroja cercana actúa como una sonda suave para tejidos profundos: menor dispersión permite una penetración cerebral más profunda; menor absorción significa daño térmico mínimo sin perjudicar las neuronas.
Tres ventajas fundamentales de la microscopía de dos fotones
- Campeón de la imagen de tejidos profundos: La profundidad de imagen alcanza cientos de micrómetros, observando directamente las neuronas corticales.
- Fototoxicidad ultrabaja: La excitación ocurre solo en el punto focal — las células circundantes no sufren daño, permitiendo imagen continua durante horas.
- Relación señal-ruido ultraalta: Sin interferencia de fondo; imágenes cristalinas con máximo contraste.
Importancia para la neurociencia
Mediante la «excitación simultánea de dos fotones», la microscopía de dos fotones logra imagen profunda, de bajo daño, alta resolución y en tejido vivo — la columna vertebral fundamental del hardware para observar el cerebro. Transforma la investigación de la anatomía estática a la función dinámica: observar neuronas disparando en tiempo real, rastrear cambios en la conectividad sináptica y descifrar cómo operan las redes neuronales.
2. Imagen de calcio — Hacer visible la actividad neuronal como luz
Con la microscopía de dos fotones como base de hardware, ¿cómo vemos realmente la actividad neuronal en tiempo real?
Las neuronas transmiten información mediante señales eléctricas (potenciales de acción), pero la electricidad es invisible. Los científicos encontraron el sustituto perfecto: iones de calcio (Ca²⁺).
Cuando una neurona dispara, los iones de calcio inundan la célula. Al rastrear la concentración de calcio, los investigadores pueden determinar indirectamente: ¡esta neurona acaba de disparar!
Herramienta estrella: proteína fluorescente de calcio GCaMP
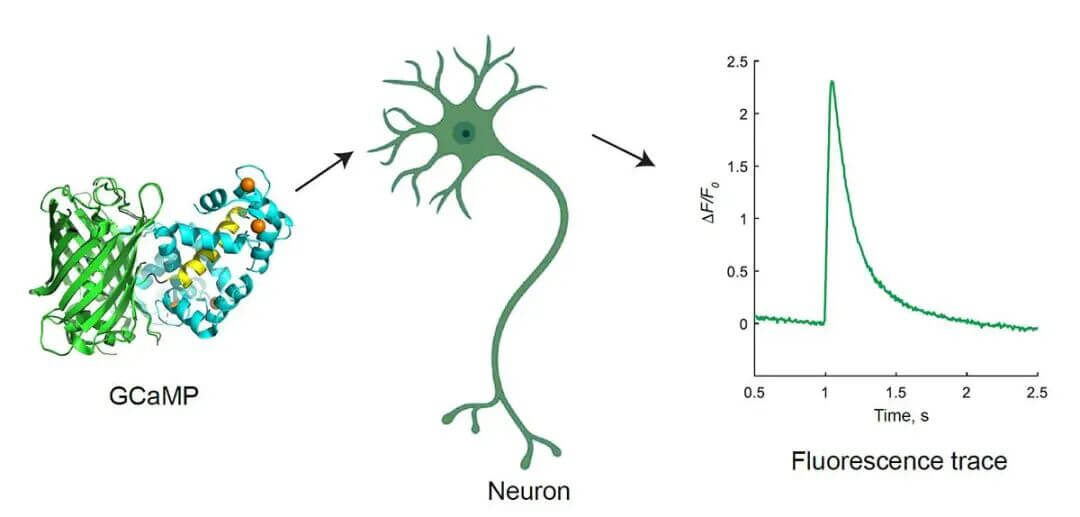
Fuente de imagen: Yan Zhang, Loren L. Looger, The Journal of Physiology, 22 de febrero de 2023
Uso exclusivo con fines académicos y educativos. Contáctenos para su eliminación si es necesario.
GCaMP es una «luz sensora de calcio» codificada genéticamente: oscura cuando no está unida al calcio, inmediatamente brillante cuando el calcio se une. Cambios en el brillo = intensidad de la actividad neuronal.
Una nota importante: señales de calcio ≠ señales eléctricas
- Señales eléctricas: ultrarrápidas, directas, escala de milisegundos
- Señales de calcio: ligeramente más lentas, indirectas, reflejan actividad poblacional
Aunque es un indicador indirecto, la imagen de calcio es simple, estable y permite la observación a gran escala — sigue siendo el enfoque predominante en la actualidad.
¿Por qué debe combinarse con la microscopía de dos fotones?
La imagen de calcio depende de la fluorescencia, y la microscopía de dos fotones destaca en imagen profunda, es suave con el tejido vivo y ofrece resolución ultraalta. Juntas, permiten la observación simultánea de la actividad dinámica de cientos de neuronas dentro de un cerebro de ratón vivo.
Tres escenarios experimentales clásicos
- Procesamiento de información sensorial: Mostrar imágenes o reproducir sonidos a ratones y observar qué neuronas se activan.
- Codificación de tareas conductuales: Rastrear cómo el cerebro orquesta acciones mientras los ratones corren o toman decisiones.
- Remodelación del aprendizaje y la memoria: Tras entrenamiento repetido, los patrones de actividad neuronal cambian — registrando cómo el cerebro se «recablea» a sí mismo.
3. Sistema de fijación de cabeza — Mantener quietos a los ratones para la imagen
El mayor desafío: cualquier movimiento desenfoca la imagen
La imagen in vivo es más vulnerable a los artefactos de movimiento, pero los ratones simplemente no se quedan quietos. La solución: diseñar un sistema de fijación de cabeza.
Concepto central: fijar la cabeza, preservar la capacidad conductual
Tres componentes centrales del sistema
- Anillo de cabeza (Headring): Implantado quirúrgicamente en el cráneo del ratón, proporciona una «interfaz de fijación» estable.
- Marco de fijación: Estructura mecánica de alta precisión que bloquea la cabeza en su lugar con posicionamiento repetible.
- Plataforma conductual: Cintas de correr o discos giratorios que permiten a los ratones correr y pensar normalmente con la cabeza fijada.
¿Por qué es esencial la imagen en estado despierto?
La anestesia suprime profundamente la actividad neuronal — lo que se ve no es el verdadero estado del cerebro. La neurociencia moderna exige datos de sujetos despiertos, con comportamiento libre, realizando actividad real.
Flujo de trabajo experimental estándar
1. Cirugía: Implantar anillo de cabeza + ventana craneal
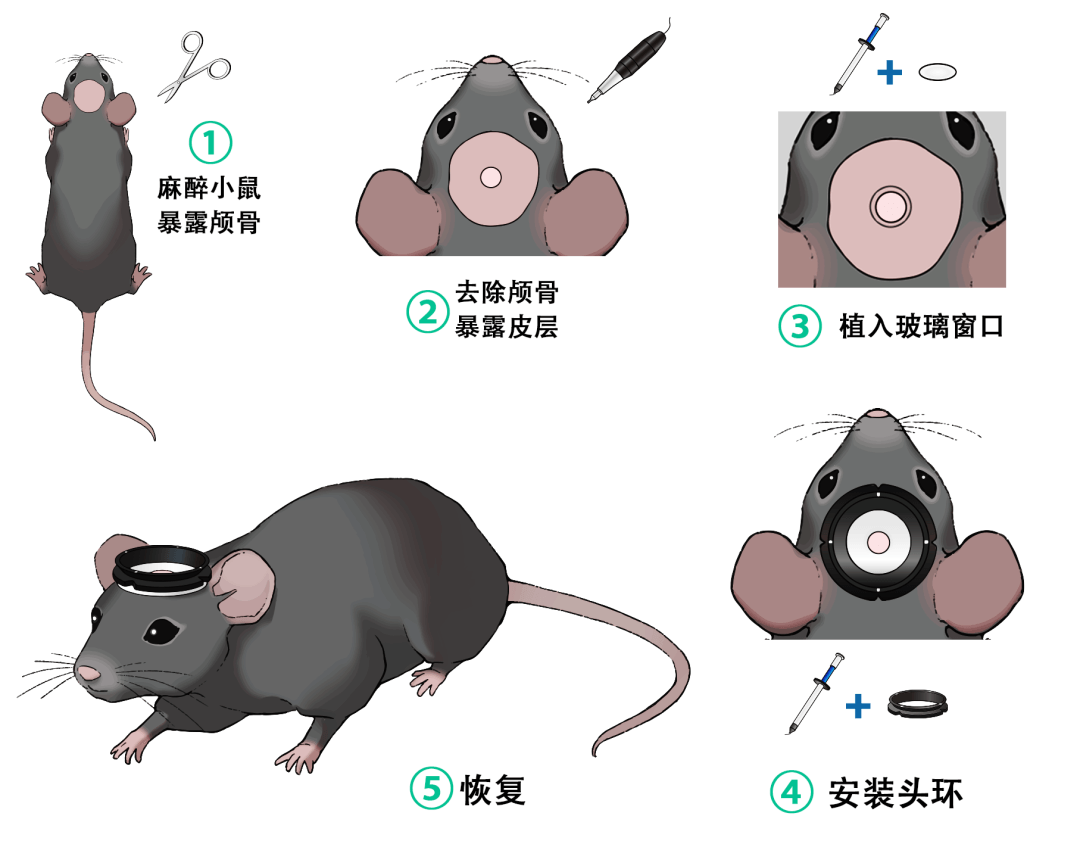
2. Recuperación: Esperar la cicatrización de la herida
3. Entrenamiento: Habituar al ratón al entorno de fijación
4. Imagen: Registro estable de la actividad neuronal

El sistema de fijación de cabeza completa el eslabón final. Mediante tecnología de imagen → comportamiento animal → actividad neuronal, podemos estudiar cómo el cerebro impulsa el comportamiento en tiempo real — y a través de este circuito de retroalimentación, lograr progresivamente el control inverso.
Sobre nosotros
SITRANTECH lleva más de cinco años profundamente involucrada en ingeniería biomédica, colaborando estrechamente con laboratorios de primera línea. Tendemos un puente entre la «visión experimental» y la «realidad ingenieril» — ofreciendo tanto equipos estandarizados de comportamiento in vivo con precisión micrométrica (como sistemas de fijación de cabeza para ratones despiertos) como servicios de ingeniería personalizada ágiles para transformar sus ideas de investigación únicas en datos experimentales fiables. Nuestra misión es simple: impulsar el descubrimiento científico mediante la ingeniería de precisión, llevando la innovación del laboratorio a las aplicaciones del mundo real.
Publicado originalmente en Cuenta Oficial SITRANTECH WeChat









