Nous avons toujours été curieux : comment fonctionnent exactement les neurones du cerveau ? Avant les technologies d'imagerie avancées, c'était comme regarder le monde à travers un verre dépoli — flou, superficiel et endommageant pour les échantillons. Puis une « combinaison en or » est apparue : microscopie biphotonique + imagerie calcique + système de fixation de tête, permettant aux scientifiques de voir pour la première fois un cerveau vivant, éveillé et pensant.
Pourquoi les microscopes conventionnels ne peuvent-ils pas voir un cerveau vivant ?
Limites de la microscopie à fluorescence traditionnelle
🔻 La lumière éclaire toute la couche → fort bruit de fond
🔻 Plus le tissu est épais, moins on voit → profondeur d'imagerie limitée
🔻 L'illumination prolongée endommage les cellules → phototoxicité élevée
Les exigences fondamentales des neurosciences sont précisément : imager le tissu vivant, en profondeur, sur de longues périodes, en capturant l'activité réelle. La microscopie traditionnelle en est tout simplement incapable — jusqu'à l'avènement de la microscopie biphotonique.
1. Microscopie biphotonique — La révolution optique de l'imagerie cérébrale
Principe fondamental — Deux photons faibles excitent simultanément la fluorescence au lieu d'un photon fort
- Fluorescence conventionnelle : 1 photon haute énergie → couche aléatoire → toute la couche fluoresce
- Biphotonique : 2 photons basse énergie → doivent frapper le même point simultanément → alors seulement la fluorescence est excitée
La probabilité que deux photons coïncident dans le temps et l'espace est extrêmement faible (nécessitant un chevauchement en 10-16–10-18 secondes), ne se produisant que dans l'infime région focale du laser. C'est pourquoi les microscopes biphotoniques exigent des sources lumineuses exceptionnelles. Le laser principalement utilisé aujourd'hui est le laser pulsé femtoseconde titane-saphir, qui délivre des impulsions ultra-denses à l'échelle femtoseconde, augmentant considérablement la probabilité d'excitation biphotonique simultanée au point focal. L'apparition du laser femtoseconde est ce qui a rendu l'imagerie biphotonique concrètement réalisable.
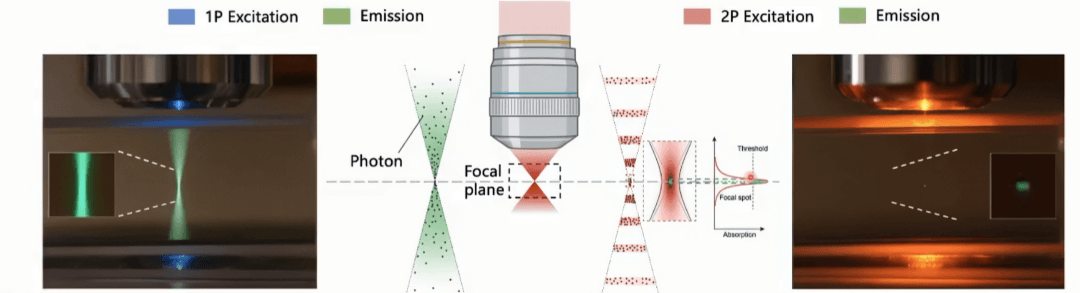
Source de l'image : « 1P vs 2P fluorescence imaging » par Steve Ruzin et Holly Aaron
Utilisée uniquement à des fins académiques et éducatives. Contactez-nous pour toute demande de suppression.
Caractéristiques clés de l'imagerie biphotonique
- Sectionnement optique intrinsèque : pas besoin de sténopé confocal — capacité de balayage couche par couche intégrée.
- Fond quasi nul : les régions hors du foyer restent totalement sombres, produisant des images exceptionnellement propres.
- Véritable imagerie 3D : en variant la profondeur focale, les couches successives peuvent être balayées et les structures cérébrales 3D reconstruites.
Pourquoi la microscopie biphotonique utilise-t-elle des lasers proche infrarouge ? (650–1100 nm)
La lumière proche infrarouge agit comme une sonde douce pour les tissus profonds : moins de diffusion permet une pénétration cérébrale plus profonde ; une absorption plus faible signifie des dommages thermiques minimaux sans nuire aux neurones.
Trois avantages fondamentaux de la microscopie biphotonique
- Champion de l'imagerie en profondeur : la profondeur d'imagerie atteint des centaines de micromètres, permettant l'observation directe des neurones corticaux.
- Phototoxicité ultra-faible : l'excitation ne se produit qu'au point focal — les cellules environnantes restent intactes, permettant une imagerie continue pendant des heures.
- Rapport signal/bruit ultra-élevé : pas d'interférence de fond ; images d'une clarté cristalline avec un contraste maximal.
Importance pour les neurosciences
Grâce à l'« excitation biphotonique simultanée », la microscopie biphotonique réalise une imagerie profonde, peu dommageable, haute résolution et en tissu vivant — l'épine dorsale matérielle fondamentale pour l'observation du cerveau. Elle transforme la recherche, passant de l'anatomie statique à la fonction dynamique : observer les neurones décharger en temps réel, suivre les changements de connectivité synaptique et décoder le fonctionnement des réseaux neuronaux.
2. Imagerie calcique — Rendre l'activité neuronale visible sous forme de lumière
Avec la microscopie biphotonique comme base matérielle, comment voyons-nous réellement l'activité neuronale en temps réel ?
Les neurones transmettent l'information via des signaux électriques (potentiels d'action), mais l'électricité est invisible. Les scientifiques ont trouvé le substitut parfait : les ions calcium (Ca²⁺).
Lorsqu'un neurone décharge, les ions calcium affluent dans la cellule. En suivant la concentration de calcium, les chercheurs peuvent déterminer indirectement : ce neurone vient de décharger !
Outil vedette : la protéine fluorescente calcique GCaMP
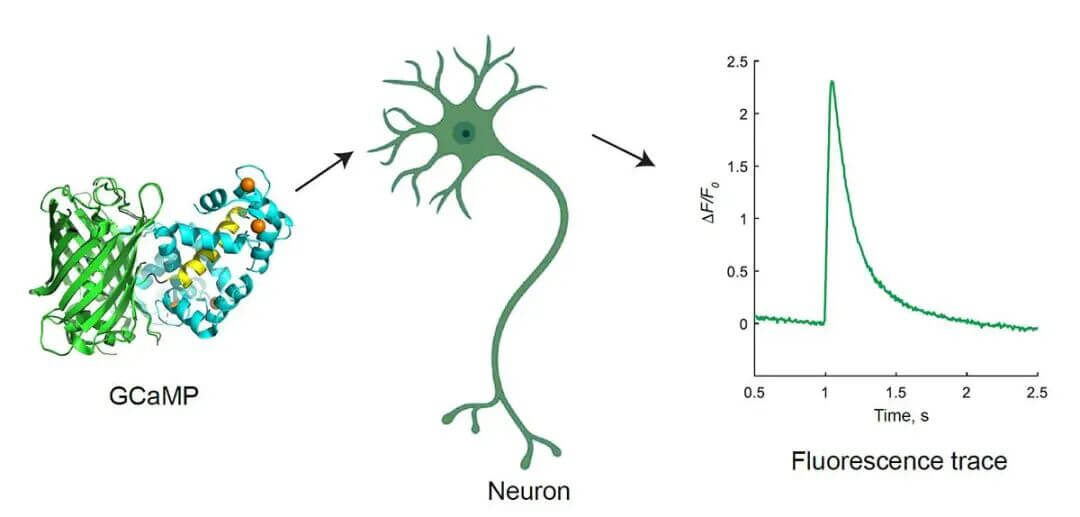
Source de l'image : Yan Zhang, Loren L. Looger, The Journal of Physiology, 22 février 2023
Utilisée uniquement à des fins académiques et éducatives. Contactez-nous pour toute demande de suppression.
GCaMP est un « capteur lumineux de calcium » encodé génétiquement : sombre lorsqu'il n'est pas lié au calcium, immédiatement brillant lorsque le calcium se lie. Les variations de luminosité = l'intensité de l'activité neuronale.
Note importante : signaux calciques ≠ signaux électriques
- Signaux électriques : ultra-rapides, directs, à l'échelle de la milliseconde
- Signaux calciques : légèrement plus lents, indirects, reflétant l'activité de population
Bien qu'indicateur indirect, l'imagerie calcique est simple, stable et permet l'observation à grande échelle — restant l'approche dominante aujourd'hui.
Pourquoi faut-il l'associer à la microscopie biphotonique ?
L'imagerie calcique dépend de la fluorescence, et la microscopie biphotonique excelle dans l'imagerie profonde, est douce pour les tissus vivants et offre une résolution ultra-haute. Ensemble, elles permettent l'observation simultanée de l'activité dynamique de centaines de neurones dans un cerveau de souris vivante.
Trois scénarios expérimentaux classiques
- Traitement de l'information sensorielle : montrer des images ou diffuser des sons aux souris et observer quels neurones sont activés.
- Encodage des tâches comportementales : suivre comment le cerveau orchestre les actions lorsque les souris courent ou prennent des décisions.
- Remodelage de l'apprentissage et de la mémoire : après un entraînement répété, les schémas d'activité neuronale changent — enregistrant le « recâblage » du cerveau.
3. Système de fixation de tête — Maintenir les souris immobiles pour l'imagerie
Le plus grand défi : tout mouvement brouille l'image
L'imagerie in vivo est la plus vulnérable aux artefacts de mouvement, mais les souris ne restent tout simplement pas immobiles. La solution : concevoir un système de fixation de tête.
Concept clé : fixer la tête, préserver la capacité comportementale
Trois composants clés du système
- Anneau crânien (Headring) : implanté chirurgicalement sur le crâne de la souris, il fournit une « interface de fixation » stable.
- Cadre de fixation : une structure mécanique de haute précision qui verrouille la tête en place avec un positionnement reproductible.
- Plateforme comportementale : tapis roulants ou disques rotatifs permettant aux souris de courir et penser normalement avec la tête fixée.
Pourquoi l'imagerie en état éveillé est-elle essentielle ?
L'anesthésie supprime profondément l'activité neuronale — ce que l'on voit ne reflète pas le véritable état du cerveau. Les neurosciences modernes exigent des données provenant de sujets éveillés, se comportant librement et engagés dans une activité réelle.
Flux de travail expérimental standard
1. Chirurgie : implanter l'anneau crânien + la fenêtre crânienne
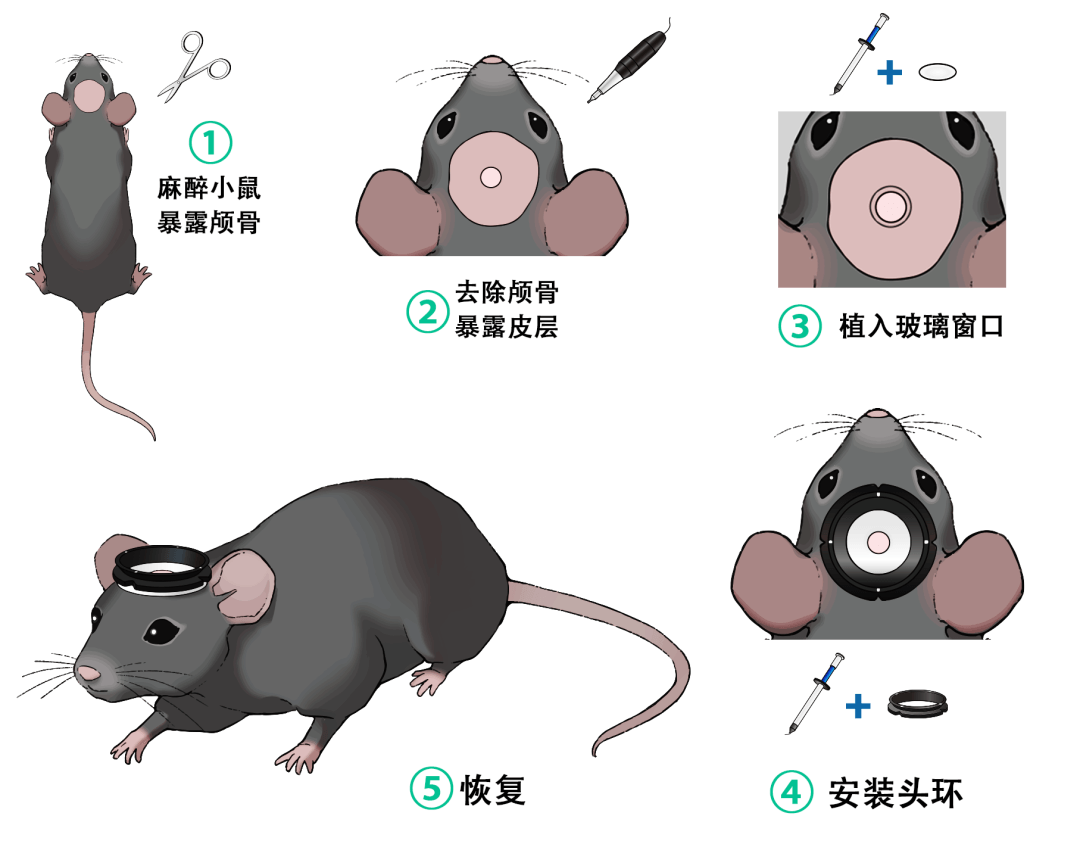
2. Récupération : attendre la cicatrisation de la plaie
3. Entraînement : habituer la souris à l'environnement de fixation
4. Imagerie : enregistrement stable de l'activité neuronale

Le système de fixation de tête achève le dernier maillon. Via technologie d'imagerie → comportement animal → activité neuronale, nous pouvons étudier comment le cerveau pilote le comportement en temps réel — et grâce à cette boucle de rétroaction, réaliser progressivement un contrôle inverse.
À propos de nous
SITRANTECH est profondément engagée dans l'ingénierie biomédicale depuis plus de cinq ans, collaborant étroitement avec des laboratoires de pointe. Nous comblons le fossé entre « vision expérimentale » et « réalité d'ingénierie » — en proposant à la fois des équipements comportementaux in vivo standardisés à précision micrométrique (tels que les systèmes de fixation de tête pour souris éveillées) et des services d'ingénierie sur mesure agiles pour transformer vos idées de recherche uniques en données expérimentales fiables. Notre mission est simple : favoriser la découverte scientifique grâce à l'ingénierie de précision, en portant l'innovation du laboratoire aux applications concrètes.
Publié initialement sur Compte Officiel SITRANTECH WeChat









