我們總好奇:大腦裡的神經元,到底是怎麼工作的?在沒有先進成像技術之前,這就像隔著毛玻璃看世界——模糊、淺層、還容易損傷樣本。直到一套「黃金組合」出現:雙光子顯微鏡 + 鈣成像 + 頭固定系統,讓科學家第一次真正看見活著、清醒、在思考的大腦。
為什麼普通顯微鏡,看不見活的大腦?
傳統螢光顯微鏡的短板
🔻 光一照就「整層都亮」 → 背景很強
🔻 組織越厚,越看不清 → 觀察深度較淺
🔻 光照久了,細胞會「受傷」 → 光毒性強
神經科學最核心的需求,恰恰是:看活體、看深層、看長時間、看真實活動。傳統顯微鏡,完全做不到,直到雙光子顯微鏡的出現。
1、雙光子顯微鏡——大腦成像的「光學革命」
雙光子核心原理——用兩個弱光子同時激發,代替一個強光子去激發螢光
- 普通螢光:1個高能光子 → 隨機層 → 全層發光
- 雙光子:2個低能光子 → 必須同時撞到同一點 → 才能激發螢光
想要實現2個光子在時間和空間上重合的機率極低(需要兩個光子在10-16~10-18 sec內重合),只發生在雷射焦點那極小的區域。所以,雙光子顯微鏡所使用的光源要求也十分高。目前主要使用的雷射器為——鈦-藍寶石飛秒脈衝雷射器,它可以在飛秒級別發出高密度脈衝式雷射,大大提高了兩個光子在焦點同時激發的機率,飛秒雷射器的出現使得雙光子成像成為現實。
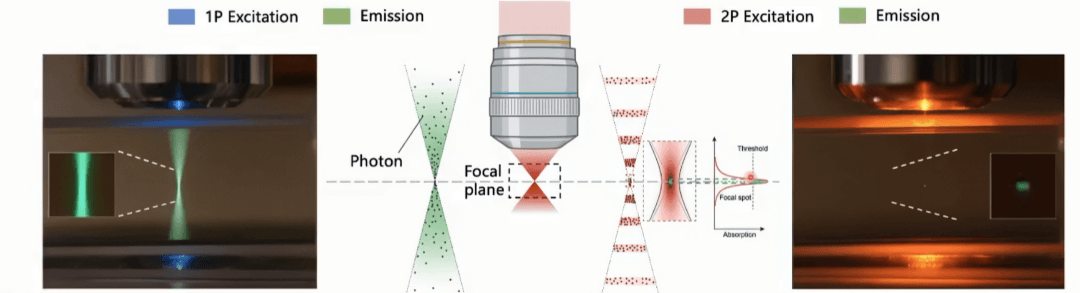
圖片來源:「1P vs 2P fluorescence imaging」by Steve Ruzin and Holly Aaron
僅用於學術科普交流,如有侵權請聯繫刪除
雙光子成像的特點
- 天然光學切片:不用共聚焦的針孔濾鏡,自帶「層掃」能力。
- 背景幾乎為零:非焦點區域完全不亮,影像極度乾淨。
- 真·三維成像:改變焦點深度,就能逐層掃描,重建大腦立體結構。
雙光子光源為什麼用紅外雷射?(650–1100 nm)
近紅外光就像溫柔的深層探針:散射更少,能鑽進大腦更深層,吸收更少,熱損傷極小,不傷害神經元。
雙光子三大核心優勢
- 深層成像王者:成像深度可達數百微米,直接觀測大腦皮層神經元。
- 超低光毒性:只在焦點激發,周圍細胞毫髮無傷,可連續成像數小時。
- 超高訊噪比:無背景干擾,畫面清晰、對比度拉滿。
對神經科學的意義
雙光子顯微鏡依靠「雙光子同步激發」,實現深層、低損、高清、活體成像,是觀測大腦的「硬核硬體基礎」。它把研究從靜態解剖,推向動態功能:即時看神經元放電、追蹤突觸連接變化、解析大腦神經網路如何運轉。
2、鈣成像——把「神經活動」變成「看得見的光」
有了雙光子顯微鏡這個硬體基礎,我們怎麼看見神經的即時活動呢?
神經元靠電訊號(動作電位)傳遞資訊,但電是看不見的。科學家找到一個完美「替身」:鈣離子(Ca²⁺)。
當神經元興奮放電時,鈣離子會大量衝進細胞。只要能追蹤鈣離子濃度,就能間接判斷:這個神經元,剛才活動了!
明星工具:GCaMP 鈣螢光蛋白
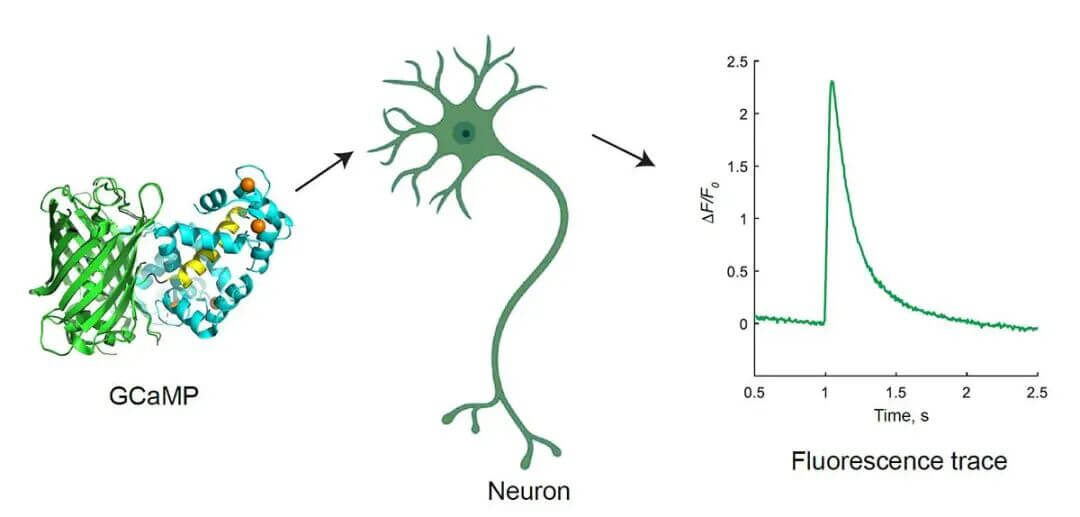
圖片來源:Yan Zhang, Loren L. Looger, The Journal of Physiology, 22 February 2023
僅用於學術科普交流,如有侵權請聯繫刪除
它是一個基因編碼的「鈣感應燈」:不結合鈣時暗,結合鈣時立刻變亮,亮度變化 = 神經元活動強度。
但是需要說明:鈣訊號 ≠ 電訊號
- 電訊號:超快、直接、毫秒級
- 鈣訊號:稍慢、間接、反映群體活動
雖然是間接指標,但簡單、穩定、可大規模觀測,至今仍是主流。
為什麼必須搭配雙光子?
鈣成像依賴螢光,而雙光子能拍深層、對活體友好、解析度超高。兩者一結合,就能在活鼠大腦裡,同時看幾百個神經元的動態活動。
三大經典實驗場景
- 感覺資訊處理:給小鼠看圖片、聽聲音,看哪些神經元被激活。
- 行為任務編碼:小鼠跑步、做決策,追蹤大腦如何指揮動作。
- 學習與記憶重塑:反覆訓練後,神經元活動模式改變,記錄大腦「重新佈線」。
3、頭固定系統——讓小鼠「乖乖配合」成像實驗
最大難題:動物一動,影像全糊
活體成像最怕運動偽影,但小鼠不可能乖乖不動,解決方案就是設計——頭固定系統。
核心理念:固定頭部,盡量保留小鼠的行為能力
系統三大核心組件
- 頭環(Headring):手術植入小鼠頭骨,提供穩定「固定介面」。
- 固定支架:高精度機械結構,鎖死頭部,可重複定位。
- 行為平台:跑步機、跑盤,讓小鼠在固定狀態下正常跑、正常思考。
為什麼一定要「清醒成像」?
麻醉會強烈抑制神經活動,看到的不是真實大腦狀態。現代神經科學,只認清醒、自由行為、真實活動的數據。
標準實驗流程
1. 手術:植入頭環 + 顱窗
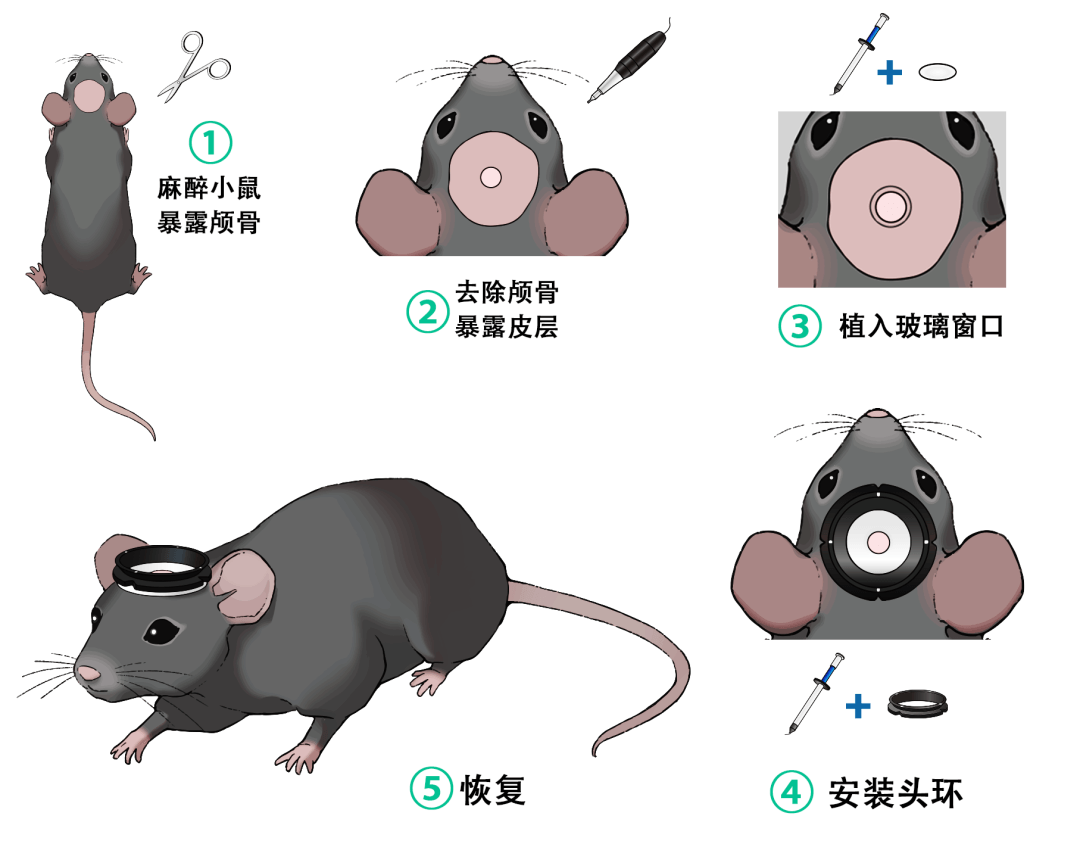
2. 恢復:等待傷口癒合
3. 訓練:讓小鼠習慣固定環境
4. 成像:穩定記錄神經元活動

頭固定系統打通了最後一環,透過成像技術 → 動物行為 → 神經活動,讓我們能研究:大腦如何即時驅動行為活動,並且透過這種回饋,可以逐步實現反向控制。
關於我們
司川科技 (SITRANTECH) 深耕生物醫學工程領域,與一線實驗室深度協作已逾五年。我們致力於彌合「實驗構想」與「工程實現」之間的鴻溝——既提供微米級精度的標準化在體行為學設備(如清醒小鼠頭固定系統),亦透過敏捷的客製化工程服務,將您獨特的科研靈感轉化為可靠的實驗數據。我們的使命很簡單:以精密工程助力科研發現,讓創新從實驗室走向真實應用。
本文首發於 SITRANTECH 司川科技微信公眾號










